La bio-impression, futur de la médecine sur-mesure ?
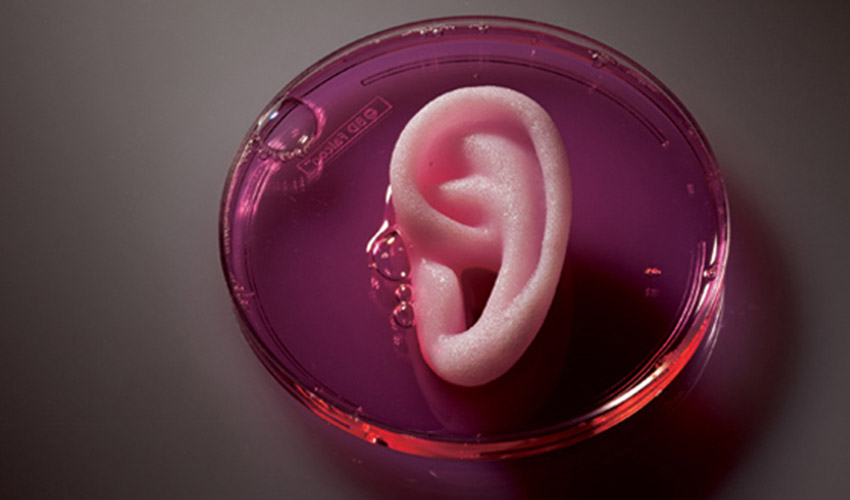
La bio-impression 3D s’impose rapidement comme l’un des secteurs les plus innovants de l’industrie de l’impression 3D. Jusqu’à récemment, ce marché était principalement dominé par l’Amérique du Nord, mais il suscite désormais un intérêt croissant auprès des entreprises, des laboratoires et des universités à travers le monde. Cette technologie permet de combiner cellules et biomatériaux, qui sont déposés couche par couche grâce à l’impression 3D, pour produire des pièces et des implants aux propriétés similaires à celles des tissus naturels. Les biomatériaux disponibles sont diversifiés et leur combinaison varie en fonction des cellules utilisées et des applications visées.
L’objectif ultime dans ce domaine serait de parvenir à bio-imprimer un organe humain entièrement fonctionnel. Bien que la science n’ait pas encore atteint ce niveau, de nombreuses zones d’incertitude entourent encore ce processus d’impression. Cependant, les recherches progressent et les avancées deviennent de plus en plus encourageantes. Dans l’article suivant, nous examinerons ce sujet en détail et tenterons de répondre aux questions les plus courantes sur la bio-impression 3D. Nous explorerons également les différents procédés d’impression associés à cette technologie innovante.

Crédits photo : Fluid Form
Les débuts de la bio-impression
L’intérêt des chercheurs pour la bio-impression 3D a été motivé par l’ambition de créer un jour un organe humain imprimé en 3D. La demande croissante de greffes, bien supérieure au nombre de donneurs disponibles, a rendu cette technologie particulièrement prometteuse. La bio-impression 3D pourrait apporter une solution durable à ce défi majeur. Mais comment cette technologie a-t-elle vu le jour ?
Le concept de la bio-impression est apparu en 1988, grâce au Dr Robert J. Klebe de l’Université du Texas, qui a introduit la méthode du Cytoscribing. Cette technique utilisait une imprimante à jet d’encre classique pour positionner précisément des cellules et créer des tissus synthétiques en 2D et 3D. Plus tard, en 2002, le professeur Anthony Atala, de l’Université Wake Forest, a réalisé une percée en créant le premier organe bio-imprimé : un petit rein. En 2010, Organovo, le premier laboratoire spécialisé dans l’impression 3D, a vu le jour. En collaboration avec les développeurs d’Invetech, Organovo a conçu l’une des premières bio-imprimantes du marché, la NovoGen MMX. Depuis, cette entreprise s’est imposée comme un acteur clé dans le domaine, poursuivant ses recherches sur le développement de tissus, notamment osseux, et ayant déjà réussi des greffes de tissu hépatique.
En 2019, une avancée majeure a transformé le domaine de la bio-impression. Des chercheurs de l’Université de Tel-Aviv (TAU) ont réussi à imprimer en 3D un cœur à partir de cellules humaines, reproduisant parfaitement les caractéristiques immunologiques, cellulaires et anatomiques d’un patient. Bien que ce cœur ait été de la taille d’un cœur de lapin, sa complexité représentait une première mondiale. « Jusqu’ici, il était possible d’imprimer en 3D la structure d’un cœur, mais sans cellules ni vaisseaux sanguins. Nos travaux démontrent le potentiel de cette méthode pour la création personnalisée de tissus et d’organes à l’avenir », a déclaré le professeur Tal Dvir, responsable de l’étude. Dans la foulée, BIOLIFE4D a également accompli l’exploit de bio-imprimer un cœur humain miniature, devenant ainsi la première entreprise américaine à réaliser cette prouesse.

Le professeur Anthony Atala.
En 2022, des chercheurs de l’Université de Boston ont développé une innovation : une « pompe microfluidique unidirectionnelle de précision miniaturisée », surnommée miniPUMP, grâce à la bio-impression 3D. Ce dispositif se distingue par sa capacité à battre de manière autonome, à l’image d’un cœur humain, grâce à l’intégration de tissu vivant. Cette avancée représente une étape clé pour approfondir la compréhension du fonctionnement du cœur et de certaines pathologies cardiaques. Par ailleurs, d’autres projets récents ont permis la reproduction d’organes à petite échelle, témoignant des progrès constants dans ce domaine.
Cependant, une technologie d’une telle envergure n’est pas sans défis. Parmi les principaux obstacles figurent son coût élevé, qui limite souvent son développement, ainsi que les questions éthiques qu’elle soulève. Malgré cela, l’émergence de nouvelles méthodes, parfois plus abordables, laisse entrevoir des perspectives prometteuses.

miniPUMP (Crédits photo : Jackie Ricciardi)
La bio-impression 3D : procédés et techniques
Comme mentionné précédemment, la bio-impression 3D offre de nombreuses applications en médecine et en recherche médicale. Le processus commun à ces utilisations repose sur la collecte et le traitement de données, qui sont ensuite transformées pour concevoir un modèle spécifique. Lorsqu’il s’agit de développer des tissus et des implants fonctionnels reproduisant les caractéristiques morphologiques et architecturales humaines, il est souvent indispensable de s’appuyer sur l’anatomie du patient. Ce processus peut être résumé en plusieurs étapes principales :
- Acquisition des données : collecter des images (TDM, IRM, etc.), ainsi que des tissus et cellules du patient.
- Reconstruction : utiliser des logiciels et des techniques de bio-ingénierie pour modéliser les tissus endommagés ou les parties à reproduire.
- Sélection des biomatériaux : choisir les matériaux les plus adaptés aux besoins spécifiques du projet.
- Préparation des matériaux biologiques : intégrer les cellules dans le biomatériau pour produire le matériau de fabrication.
- Choix de la technologie d’impression : déterminer la méthode d’impression la plus adaptée à l’application finale.
Concernant les technologies spécifiques, trois principales méthodes de bio-impression 3D sont largement utilisées et reconnues au niveau international : la bio-impression à jet d’encre, l’extrusion et l’utilisation du laser. En plus de ces techniques, d’autres méthodes plus expérimentales ou développées dans le cadre de recherches particulières existent, et seront présentées ci-dessous.
Impression 3D bio par jet d’encre
L’une des technologies les plus répandues en bio-impression 3D est la technologie jet d’encre, qui s’inspire du processus d’impression Inkjet traditionnel des imprimantes 2D. En effet, il est possible de convertir une imprimante classique en bio-imprimante 3D. Cette méthode consiste à déposer des gouttes d’encre biologique, ou biomatériau, couche par couche sur un support hydrogel ou une boîte de Petri. Elle repose sur deux principales techniques : thermique et piézoélectrique, toutes deux utilisant un mécanisme biotinique.
Le procédé thermique fonctionne en chauffant un système qui génère des bulles d’air. Celles-ci se contractent, créant la pression nécessaire pour expulser les gouttes d’encre biologique. En revanche, la méthode piézoélectrique utilise un cristal céramique piézoélectrique dans la buse. Ce matériau se dilate ou se contracte lorsqu’il est soumis à un courant électrique, ce qui pousse l’encre hors de la buse. Toutefois, l’un des principaux inconvénients de cette technologie est qu’elle peut endommager les membranes cellulaires, ce qui entraîne une faible teneur en cellules dans les encres produites.

Technique de bio-impression 3D par jet d’encre.
Les chercheurs ont réalisé d’importants progrès dans la modélisation des molécules, des cellules et des organes grâce à l’impression à jet d’encre. Des molécules comme l’ADN ont été reproduites avec succès, facilitant ainsi l’étude et le traitement du cancer. Les cellules impliquées dans le cancer du sein peuvent également être imprimées tout en conservant leurs fonctions, offrant ainsi de grandes possibilités pour la création de structures tissulaires vivantes.
Organovo utilise l’impression à jet d’encre pour produire des tissus humains fonctionnels, en se concentrant particulièrement sur la reproduction des tissus hépatiques humains. Leur objectif est de réparer les parties endommagées du foie en implantant des tissus bio-imprimés, ce qui permettrait de prolonger la vie de l’organe en attendant une transplantation, un processus qui peut parfois prendre plusieurs années.
Bio-impression par extrusion
Cette méthode est particulièrement populaire en raison de sa simplicité d’exécution et de ses coûts relativement faibles. Elle repose sur l’extrusion d’une solution composée de biomatériaux et de cellules du patient. Le processus consiste à imprimer le modèle ou le tissu souhaité, couche après couche. Parmi ses avantages, on note le fait que l’impression se déroule à température ambiante, qu’elle permet une incorporation cellulaire directe et qu’elle assure une distribution homogène des cellules. Certaines des bio-imprimantes les plus utilisées, comme la Bioplotter et l’EnvisionTec, emploient cette technique, qui est considérée comme la prochaine étape dans l’évolution de la bio-impression par jet d’encre.

Bio-imprimante 3D de Allevi.
Bio-impression 3D basée sur laser
Cette méthode utilise un laser comme source d’énergie pour déposer des biomatériaux sur un récepteur. Elle consiste en une source laser, un ruban recouvert de matériaux biologiques et un récepteur. Les rayons laser frappent la bande, évaporant les matières biologiques liquides, qui sont ensuite transférées sous forme de gouttelettes vers le récepteur. Ces gouttelettes contiennent un biopolymère qui favorise l’adhésion cellulaire et stimule la croissance des cellules. Comparée à d’autres technologies d’impression additive, la bio-impression 3D assistée par laser présente des avantages uniques, notamment l’absence de buse et de contact direct, ce qui permet d’imprimer des cellules avec une grande précision et de contrôler le dépôt des gouttelettes de biomatériaux. Toutefois, cette technologie comporte des inconvénients, notamment des coûts élevés qui limitent son adoption et sa diffusion à grande échelle.
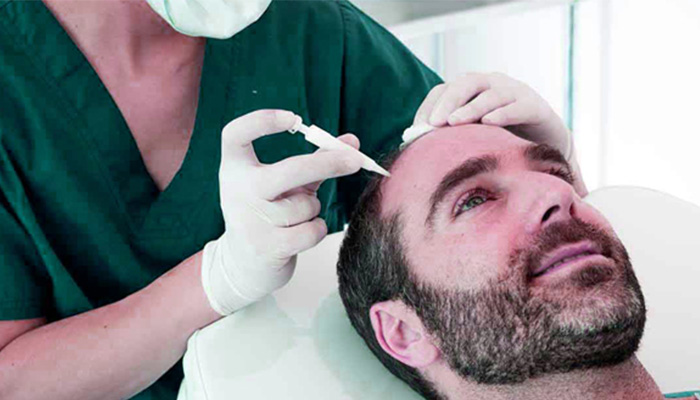
Poietis utilise la bio-impression dans le développement des follicules pileux pour mettre fin à l’alopécie.
Poietis, leader français de la bio-impression 3D, a lancé un programme de reproduction capillaire en partenariat avec L’Oréal. La société utilise une technologie de bio-impression 3D assistée par laser, permettant de déposer les cellules avec précision, selon un ordre spécifique. L’objectif est de recréer un follicule pileux pour stimuler la croissance des cheveux, offrant ainsi une alternative potentielle aux hommes et aux femmes souffrant de calvitie. Poietis est également reconnue pour avoir développé Poieskin, un modèle de peau humaine entièrement conçu par bio-impression 3D.
Autres techniques et nouveautés en bio-impression 3D
Stéréolithographie
La technologie de stéréolithographie repose sur la solidification d’un photopolymère par exposition à la lumière, offrant la plus grande précision parmi les techniques de fabrication additive. En bio-impression, elle peut être utilisée pour imprimer des hydrogels sensibles à la lumière. Bien que cette technologie présente de nombreux avantages, elle est encore en développement en raison de plusieurs défis, tels que la disponibilité limitée de polymères biocompatibles et biodégradables, les effets potentiellement nuisibles et l’incapacité d’éliminer facilement la structure de support.

Tissu bio-imprimé en 3D
Bio-impression par ondes acoustiques
Développée par l’Université Carnegie Mellon, l’Université d’État de Pennsylvanie et le MIT, cette technologie utilise un dispositif microfluidique qui permet de manipuler des cellules ou des particules à l’aide d’ondes sonores de surface. Grâce à cet appareil, les chercheurs peuvent contrôler le point de rencontre des ondes le long des trois axes. À ces points de rencontre, les ondes créent un nœud de capture 3D qui permet d’attraper des cellules individuelles. Ces cellules sont ensuite collectées pour former des motifs en 2D, puis en 3D. Cette approche globale se distingue par sa précision de mouvement élevée.
Au fil du temps, cette technologie a connu de nombreux progrès et de nouvelles applications ont rapidement émergé. Par exemple, l’Université du Nord-Ouest de l’Illinois a réussi à imprimer en 3D un ovaire, et en Suède, des chercheurs ont imprimé des tissus cartilagineux humains. Bien que ces avancées en médecine aient suscité des discussions et des spéculations sur l’avenir, un autre aspect important n’a pas encore été pleinement abordé : les implications éthiques liées à cette technologie.
La technique SWIFT
Des chercheurs de l’Institut Wyss d’ingénierie biologique de Harvard ont mis au point une nouvelle méthode de bio-impression appelée SWIFT (Sacrificial Writing Into Functional Tissue). Comme son nom l’indique, cette technique permet la bio-impression de vaisseaux sanguins dans des tissus vivants. Autrement dit, elle consiste à imprimer en 3D des canaux vasculaires dans des matrices vivantes composées de blocs de construction d’organes dérivés de cellules souches (OBB).
Plutôt que d’imprimer en 3D l’ensemble des cellules d’un organe, SWIFT se concentre sur l’impression des vaisseaux nécessaires pour soutenir un tissu vivant composé d’OBB. Ces structures peuvent potentiellement être utilisées à des fins thérapeutiques pour réparer et remplacer des organes humains grâce à des cultures de laboratoire à base des propres cellules du patient. Dans une expérience, les tissus organiques imprimés avec des canaux vasculaires intégrés grâce à SWIFT sont restés vivants, tandis que ceux cultivés sans ces canaux ont subi une mort cellulaire en seulement 12 heures.
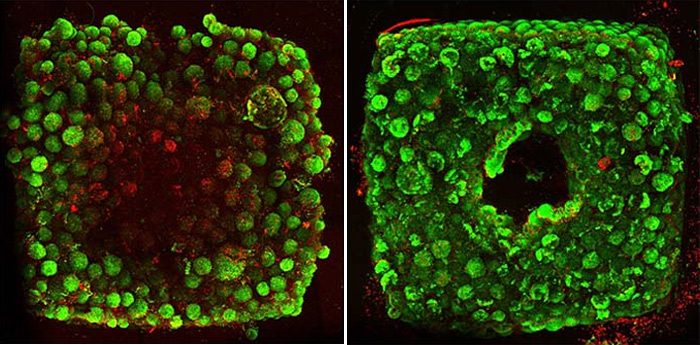
Les tissus d’organes spécifiques imprimés avec des canaux vasculaires SWIFT sont restés viables (à droite), tandis que les tissus cultivés sans ces canaux ont connu la mort cellulaire en 12 heures (à gauche).
Le futur de la bio-impression 3D en médecine
Les techniques biomédicales ont pour objectif de promouvoir une médecine personnalisée, permettant aux médecins d’adapter les traitements aux besoins spécifiques de chaque patient. Parmi les applications principales de la bio-impression 3D, on trouve la reproduction in vitro de tissus pour les tests de médicaments et l’étude de maladies particulières. Cette approche permet de réduire l’utilisation des animaux pour les expérimentations et d’optimiser l’efficacité des traitements en les testant sur des modèles correspondant aux caractéristiques uniques de chaque patient.
Un exemple notable est le travail de Carcinotech, qui obtient de bons résultats en imprimant en 3D des tumeurs à partir des cellules du patient et en testant des médicaments plus efficaces sur ces modèles. Cela représente une avancée importante dans le développement de thérapies anticancéreuses plus ciblées et combinées. La création d’implants ou de tissus basés sur les cellules du patient a également connu des succès cliniques. Par exemple, la société 3DBio Therapeutics fabrique des implants auriculaires à partir de hydrogels de collagène et de cellules cartilagineuses du patient.

Crédits photo : 3DBio Therapeutics
Selon les prévisions de Grand View Research, une société de recherche de marché basée à San Francisco, le marché mondial de la bio-impression devrait atteindre 4,1 milliards de dollars d’ici 2026, avec un taux de croissance annuel composé de 19,5 %.
Le domaine des matériaux devrait également connaître une expansion, grâce à des technologies comme l’intelligence artificielle (IA), qui permettent aux scientifiques de déterminer plus facilement la combinaison idéale de biomatériaux pour transformer les échafaudages médicaux en tissus. Les entreprises de bio-impression se concentreront probablement sur le développement de nouveaux biomatériaux ainsi que sur la mise en place de systèmes de bio-impression à têtes multiples pour permettre l’utilisation de plusieurs bioencres simultanément. On prévoit également des avancées dans les logiciels de bio-impression, offrant ainsi davantage de fonctionnalités aux utilisateurs.
Concernant les préoccupations actuelles et futures, au-delà des coûts associés, un débat éthique persiste autour des implications de la médecine personnalisée et de l’accès à ces traitements. Une autre difficulté éthique réside dans la complexité, voire l’impossibilité, de prouver l’efficacité et la sécurité de ces traitements. Bien qu’il soit techniquement possible de développer des organes et tissus fonctionnels pour remplacer les organes humains, il reste incertain de savoir si le corps du patient acceptera ou non ces nouveaux tissus ou organes artificiels. De plus, il est essentiel de prendre en compte la réglementation juridique qui devra être établie avant que ces innovations ne puissent être mises à la disposition des patients.
Les créateurs de la première cornée imprimée en 3D (Crédits : Université de Newcastle)
De plus, bien que les nouvelles technologies offrent de nombreuses possibilités, elles peuvent aussi être mal utilisées, et la bio-impression 3D ne fait pas exception. Si ces technologies permettent de créer des organes ou des tissus adaptés aux besoins spécifiques d’un individu, il est important de prendre en compte les conséquences négatives potentielles d’une médecine trop personnalisée. Par exemple, on pourrait envisager la création de capacités surhumaines, comme des os renforcés ou des poumons ayant une fonction oxygénante différente. De telles avancées pourraient avoir des applications intéressantes dans des secteurs comme l’armée.
Les chercheurs et scientifiques ont donc encore de nombreux défis à relever, avec l’appui des institutions et organismes compétents. Cependant, il est clair que la bio-impression 3D représente l’une des avancées les plus significatives dans le domaine médical et qu’elle pourrait constituer une véritable révolution pour l’avenir de la médecine.
Que pensez-vous de l’évolution de la bio-impression 3D ? N’hésitez pas à partager votre avis dans les commentaires de l’article. Retrouvez toutes nos vidéos sur notre chaîne YouTube ou suivez-nous sur Facebook ou LinkedIn !






On peut imrimer des organes allant jusque à quelle taille dans du gel avant d’avoir besoin de les oxygéner avec du sang? Il faudrait à mon avis fabriquer des morceaux de quelques cm3 puis les assembler le plus vite possible et y injecter du sang ou alors oxygéner directement l’organe pendant l’impression