La bioimpresión 3D y la ética, ¿cuáles son las normas actuales?

En el panorama en rápida evolución de la biotecnología, la bioimpresión 3D ha surgido como un rayo de esperanza para transformar la asistencia sanitaria y abordar retos médicos críticos. Estos incluyen el trasplante de órganos, la ingeniería de tejidos, el ensayo y desarrollo de fármacos, la medicina personalizada, la regeneración nerviosa, el modelado de enfermedades y mucho más. Esta tecnología puede revolucionar la forma en que abordamos la medicina moderna y está atrayendo cada vez más la atención de investigadores, inversores y profesionales de la salud. Sin embargo, a medida que la bioimpresión 3D evoluciona con rapidez, se ve sometida al escrutinio crítico de la consideración ética, los marcos jurídicos y los retos normativos.
Así, la necesidad de afrontar y abordar las complejidades éticas que rodean a esta nueva tecnología se hace cada vez más evidente. Para entenderlo mejor, hemos echado un vistazo al corazón de la industria de la bioimpresión, explorando su ética real que surge de la fabricación de órganos humanos artificiales. También analizaremos el controvertido uso de células madre embrionarias humanas y los riesgos potenciales asociados con las células madre pluripotentes inducidas, la digitalización, los ensayos clínicos y la experimentación con animales, entre otros. Poniendo la bioimpresión bajo el microscopio, examinaremos la intrincada interacción entre su extraordinario potencial y la acuciante necesidad de una gobernanza responsable. Navegando por estas complejidades, será importante desentrañar el delicado equilibrio entre innovación y responsabilidad ética, garantizando así que el futuro de la medicina progrese con la conciencia tranquila.
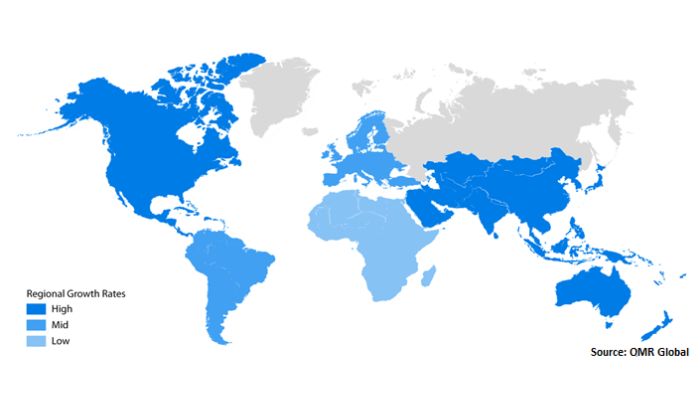
El tamaño del mercado mundial de bioimpresión 3D se contabilizó en 2.130 millones en 2022 y se prevé que alcance alrededor de 8.300 millones en 2030. (Créditos: OMR Global)
Leyes y normas universales en la biomedicina
Para entender las posibles mejoras, es esencial conocer las leyes y normas vigentes. En el ámbito de la biomedicina, estas normas forman un marco global que supervisa los aspectos médicos y biológicos, los esfuerzos de investigación y las innovaciones tecnológicas. Estas leyes y normas desempeñan un papel fundamental a la hora de garantizar la seguridad de los pacientes, abordar las consideraciones éticas, defender la integridad de la investigación y promover el progreso médico responsable. Este marco orienta varios ámbitos, cada uno con un enfoque distinto.
Por ejemplo, las áreas de Ensayos Clínicos y Ética de la Investigación asumen funciones fundacionales, supervisando la participación de seres humanos en investigaciones y ensayos clínicos. Por su parte, organismos como las Juntas de Revisión Institucional (IRB) garantizan el consentimiento informado, la protección de los derechos de los participantes y una adhesión ética inquebrantable. Al mismo tiempo, organismos reguladores gubernamentales como la FDA asumen la responsabilidad de supervisar toda la trayectoria de creación de dispositivos médicos. Tampoco hay que olvidar las leyes sobre privacidad de datos, como la GDPR y la HIPAA, que cada vez son más importantes para proteger el almacenamiento y el uso de información médica confidencial. Del mismo modo, la propiedad intelectual también debe tenerse en cuenta cuando se trata de innovaciones en este campo.
Una de las más importantes en el ámbito de la bioimpresión es la investigación con células madre. Ocupa un espacio único en la intersección del avance científico y la consideración ética, trazando límites permisibles que incluyen el complejo ámbito de las células madre embrionarias. Igualmente, el trasplante de órganos navega por el delicado equilibrio entre el bienestar del paciente y la obtención ética de órganos, fomentando un equilibrio basado en la justicia y la responsabilidad. Y, por supuesto, hay muchos más sobre diversos aspectos de la asistencia sanitaria, incluida la reproducción.
En conjunto, estas dimensiones jurídicas crean un paisaje en el que el progreso biomédico puede florecer. Las leyes y normas biomédicas, que se adaptan y evolucionan en las distintas regiones, deben ajustarse a los constantes cambios del progreso científico y a las preocupaciones de la sociedad. Este equilibrio dinámico garantiza que los avances médicos se lleven a cabo dentro de los límites de una conducta responsable y ética. De este modo, la bioimpresión no está totalmente cubierta, pero puede llevarse a cabo bajo el tapiz de la legislación de diferentes organismos.

Aunque no existe un conjunto completo de normas que supervisen todo el proceso de bioimpresión, sí hay una legislación parcial relativa a la ingeniería de tejidos y la medicina regenerativa. (Créditos: Walden University)
Leyes y normas aplicada a la bioimpresión
A continuación examinaremos cómo se aplican las leyes directamente al campo en constante evolución de la bioimpresión. De hecho, en la sección “Universal standards for tissue engineered products” de un estudio publicado por PubMed Central, se analiza la importancia de las normas universales para los productos médicos de ingeniería tisular (TEMP) a fin de garantizar una calidad uniforme en todo el mundo. Estas normas las establecen organizaciones como la Organización Internacional de Normalización (ISO) y la Sociedad Estadounidense de Pruebas y Materiales (ASTM).
Tanto la ASTM como la ISO han publicado una lista de normas para los productos médicos modificados genéticamente que abarcan diversos aspectos. Estos incluyen la clasificación, los biomateriales, las estructuras celulares y tisulares, la seguridad y las evaluaciones. Dichas normas ayudan a regular y garantizar la seguridad y calidad de los productos de ingeniería tisular desde la investigación preclínica hasta los ensayos clínicos. Además, la ISO ha colaborado con diversas organizaciones y expertos para mejorar continuamente las normas y la calidad en todo el mundo, en particular para las técnicas de fabricación aditiva utilizadas en diversos campos como la medicina.
En general, estas normas universales desempeñan un papel crucial en la validación de los productos médicos, incluidos los productos de ingeniería tisular, y garantizan su seguridad y eficacia para el uso humano. Dado que la bioimpresión es un campo en rápida evolución, las normas y las organizaciones que se ocupan de establecerlas están en continuo desarrollo. Aunque las normas específicas pueden variar, existen tendencias y aspectos generales relacionados con las normas en bioimpresión, que se refieren a:
- Normas sobre materiales. Existe la necesidad de biomateriales estandarizados que sean compatibles con los procesos de bioimpresión y seguros para su uso con células vivas. Los materiales utilizados deben tener propiedades mecánicas, biocompatibilidad y tasas de degradación adecuadas. Se están realizando esfuerzos constantes para establecer normas sobre la calidad y las características de las biotintas y los materiales de los implantes.
- Viabilidad y funcionalidad celular. Se están desarrollando normas para garantizar que las estructuras bioimpresas mantengan la viabilidad y funcionalidad celular. Los procesos de fabricación no deben comprometer la viabilidad ni el comportamiento de las células incrustadas, permitiéndoles crecer, diferenciarse y desempeñar las funciones previstas.
- Imprimibilidad y resolución. Se están estudiando directrices para el diseño e impresión de estructuras complejas. Los factores de imprimibilidad, como la resolución, el grosor de la capa y el diámetro de la boquilla, deben estandarizarse para garantizar la precisión y reproducibilidad de las estructuras bioimpresas.
- Cultivo en biorreactores. La bioimpresión suele requerir un cultivo posterior en biorreactores. Se están estudiando normas para las condiciones de cultivo, como la temperatura, la humedad, el suministro de nutrientes y la estimulación mecánica, con el fin de promover un crecimiento celular y un desarrollo tisular óptimos.
- Control de calidad y caracterización. Es esencial disponer de métodos normalizados para el control de calidad y la caracterización de las estructuras bioimpresas. Esto incluye la evaluación de la viabilidad celular, la distribución celular, la morfología tisular, las propiedades mecánicas y la funcionalidad.
- Consideraciones éticas y normativas. Se están estudiando normas para garantizar el uso responsable y seguro de las tecnologías de bioimpresión, abordando cuestiones relacionadas con la seguridad del paciente, el consentimiento y la propiedad intelectual.
- Calibración y validación de bioimpresoras. Garantizar la precisión y reproducibilidad de los procesos de bioimpresión requiere protocolos estandarizados de calibración y validación de las máquinas. Esto ayuda a obtener resultados coherentes en diferentes laboratorios y sistemas.
- Comunicación y puesta en común de datos. La comunicación normalizada de los procesos, materiales y resultados es crucial para facilitar la colaboración, la reproducibilidad y la comparación de los resultados de la investigación. El intercambio abierto de datos y métodos puede acelerar los avances en este campo.
Análisis del panorama normativo
En la actualidad, la transformación clínica de los tejidos manipulados y bioimpresos (llamada TEMP) plantea importantes retos. Uno de los principales problemas es la falta de consideraciones normativas estandarizadas a escala mundial para los TEM, lo que obliga a modificar las normas y reglamentos actuales. Las directrices reglamentarias varían de una región a otra, lo que dificulta una traducción clínica coherente de estas cuestiones. Para superar estos retos, muchos organismos reguladores adoptan un enfoque adaptativo a la hora de aprobar las TEMP, teniendo en cuenta su complejidad y falta de fiabilidad debido al uso de biomateriales y células naturales. Sin embargo, las incertidumbres científicas que rodean a las TEMP suelen provocar retrasos en su aprobación comercial.
La elección de las fuentes celulares también plantea problemas éticos, ya que se suelen utilizar células madre de donantes adultos a pesar de los posibles riesgos de seguridad a largo plazo y los problemas de inmunogenicidad. La variabilidad tras la implantación de las TEMP es otro motivo de preocupación, ya que las células metabólicamente activas en el entorno del huésped pueden provocar reacciones inmunitarias o desajustes.
La ética sobre el uso de células madre
Además, las células madre embrionarias humanas (CME) han estado durante mucho tiempo en el centro de las controversias éticas en bioimpresión debido a su derivación de embriones humanos. Aunque poseen un enorme potencial para diferenciarse en cualquier tipo de célula del cuerpo humano, su uso plantea profundas cuestiones éticas en relación con el comienzo de la vida humana y el estatus moral de los embriones. La obtención de CME humanas con fines de investigación implica la destrucción de embriones humanos, lo que da lugar a acalorados debates sobre cuándo comienza la vida y las implicaciones morales de la destrucción de los mismos. Además, la comercialización de productos derivados de CME humanas se ha topado con la resistencia de grupos religiosos y organizaciones éticas. Las consideraciones religiosas subrayan la importancia de entablar debates éticos transparentes y tener en cuenta diversas perspectivas a la hora de desarrollar directrices y normativas para la bioimpresión con CME humanas.
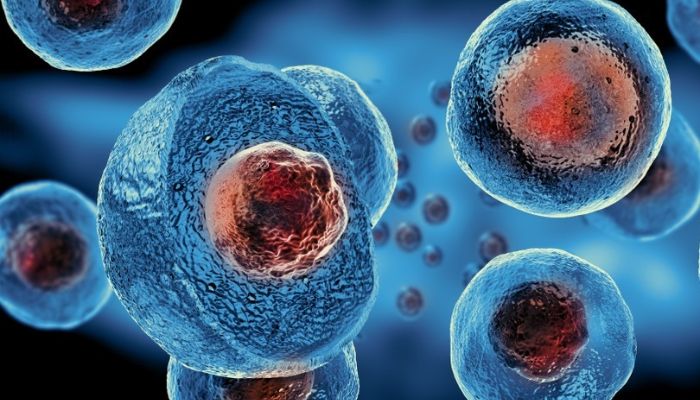
Células madre embrionarias. (Créditos: BioTechne)
Otro reto ético surge del uso de células madre pluripotentes inducidas (iPSC). Su uso en la bioimpresión 3D es muy prometedor para la medicina regenerativa. Las iPSC son células adultas que se han reprogramado genéticamente para que posean propiedades similares a las de las CME, lo que las hace capaces de diferenciarse en varios tipos celulares. Esta capacidad de generar células específicas de un paciente sin los problemas éticos asociados a las CME humanas ha convertido a las iPSC en una opción atractiva en el campo de la bioimpresión. Sin embargo, su uso no está exento de problemas éticos. Una preocupación importante es la posibilidad de reprogramación anormal durante el proceso de inducción de las iPSC. Estudios como el realizado por Keisuke Okita, profesor del Centro de Investigación y Aplicación de Células iPS de la Universidad de Kioto (Japón), han puesto de relieve la necesidad de actuar con cautela para evitar aberraciones genéticas y garantizar la seguridad de los tejidos u órganos bioimpresos.
Además, se ha observado tumorigenicidad, o producción o tendencia a producir tumores, en las iPSC durante la terapia con células madre. Un estudio de Andrew S. Lee, investigador del Instituto de Biología de Células Madre y Medicina Regenerativa de la Facultad de Medicina de la Universidad de Stanford, subraya la importancia de abordar este riesgo para evitar la formación de tumores en pacientes que reciben tratamientos basados en iPSC. “Las células madre pluripotentes (PSC), incluidas las embrionarias (ESC) y las células madre pluripotentes inducidas (iPSC), ofrecen un inmenso potencial como fuente de terapias regenerativas. Sin embargo, las cualidades intrínsecas de autorrenovación y pluripotencia que hacen que estas células sean tan prometedoras terapéuticamente también son responsables de un potencial tumorigénico igualmente fundamental”, señala Lee.
El estudio continúa mencionando que “los riesgos de tumorigenicidad de las PSC se han puesto de relieve en los últimos años en una serie de estudios con animales pequeños y grandes”. Garantizar la seguridad y eficacia de los productos derivados de iPSC es vital para mantener la confianza pública en la tecnología y proteger el bienestar de los pacientes, y sigue siendo un obstáculo para las terapias con células madre pluripotentes.
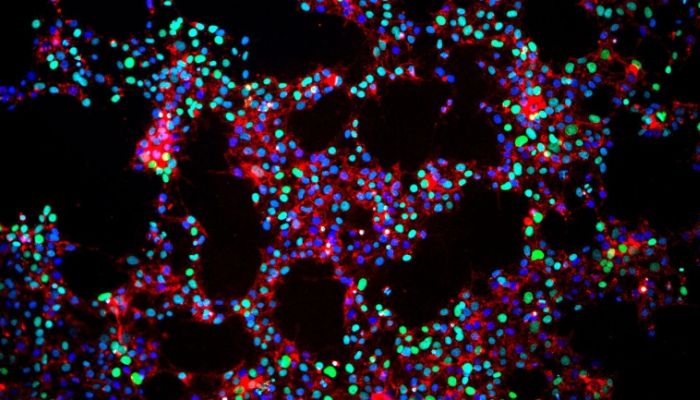
Vista microscópica de células madre pluripotentes inducidas. (Créditos: Gladstone Institute)
Aplicaciones de la propiedad
Propiedad de los modelos bioimpresos
Dado que la bioimpresión implica el uso de células madre humanas y sus componentes genéticos, se prevé que la cuestión de quién posee los derechos de propiedad sobre los modelos bioimpresos resultantes suscite ciertos debates. Este se extiende al ámbito de los datos de los pacientes y, en este contexto, al material genético de los propios pacientes. Entre las partes con intereses creados se encuentran los profesionales sanitarios, los investigadores, las empresas biotecnológicas y, sobre todo, los pacientes. Para evitar la posible aparición de un mercado ilegal de órganos bioimpresos, los expertos jurídicos y médicos tienen que colaborar para establecer unas directrices éticas claras para la gestión de estos activos. Esta colaboración tiene por objeto garantizar la equidad tanto para los pacientes como para las demás partes interesadas.
Propiedad intelectual
Niki Vermeulen, investigadora del Centro de Estudios sobre Ciencia y Tecnología (CWTS), analiza en profundidad las complejidades que entraña la formulación de un marco de propiedad intelectual para el campo de la bioimpresión. En un estudio sobre el punto de vista socioético de la impresión de órganos humanos, Niki afirma: “estas nuevas formas de impresión tendrán el mismo efecto revolucionario y democratizador que la impresión de libros en su aplicabilidad a la medicina regenerativa y a la industria”, prediciendo que las estructuras biológicas diseñadas para los individuos llegarán a estar “tan disponibles como los textos en las sociedades alfabetizadas modernas”. A continuación describe las similitudes de proceso, desarrollo y accesibilidad entre la bioimpresión 3D del siglo XXI y la imprenta del siglo XV, estableciendo varios paralelismos.
El estudio plantea un importante dilema en torno a la determinación de si la bioimpresión debe clasificarse como dispositivo médico susceptible de protección mediante patente o como procedimiento médico no patentable. Esta deliberación gira en torno a si la tecnología debe considerarse únicamente como una innovación comercialmente viable o como una práctica médica fundamental para el futuro, posiblemente incorporando ambos aspectos. Además, existe un debate en curso sobre si el acto de conceder patentes fomenta o dificulta la innovación. Y lo que es más importante, en este contexto, el resultado tiene el potencial de ejercer un impacto directo en la vida de millones de personas. Vermeulen y sus compañeros sugieren que una solución plausible a este problema pasa por la colaboración de los sectores público y privado. Este esfuerzo colectivo pretende establecer mecanismos para la creación y distribución equitativa de los beneficios de la investigación.

La propiedad sobre la bioimpresión y la propiedad intelectual es una creaciente preocupación. (Créditos: American College of Cardiology Foundation / Pixstastock)
Ensayos clínicos
Diseño de ensayos clínicos éticos
El diseño de ensayos clínicos éticos para la bioimpresión 3D resulta esencial para garantizar tratamientos personalizados y eficaces. Los criterios de inclusión y la participación de pacientes con enfermedades terminales requieren una cuidadosa evaluación ética para equilibrar los posibles riesgos y beneficios, y para defender los principios éticos en la investigación y la práctica clínica. Las dimensiones ética y jurídica de la bioimpresión 3D son de suma importancia para el desarrollo y la aplicación responsables de esta tecnología transformadora. A medida que exploramos el vasto potencial de la bioimpresión para revolucionar la atención sanitaria, es imperativo entablar debates continuos, aplicar normativas sólidas y establecer directrices éticas claras para garantizar su integración ética y beneficiosa en las prácticas sanitarias generales. Si abordamos estos retos éticos de forma proactiva, podremos allanar el camino para el avance ético de la bioimpresión, beneficiando a los pacientes y a la sociedad en su conjunto.
De cara al futuro, la bioimpresión 3D es prometedora, con la posible comercialización de modelos de tejido bioimpresos y órganos en chip en los próximos 5-8 años. Sin embargo, la comercialización de tejidos y órganos bioimpresos en 3D puede llevar décadas debido a su compleja naturaleza y composición biológica. Superar retos como la impresión de alta resolución, el cultivo de tejidos heterogéneos, el desarrollo de redes vasculares y la resolución de problemas éticos y de seguridad será crucial para aprovechar todo el potencial de la bioimpresión 3D en aplicaciones clínicas.
¿Están a la altura las prácticas actuales?
Pero la verdadera pregunta es si las normas actuales de bioimpresión cumplen su función. Parece que, aunque las prácticas actuales de bioimpresión están progresando, se enfrentan a problemas de estandarización y fiabilidad. A pesar de los avances significativos en la tecnología de bioimpresión, hay casos en los que las prácticas no alcanzan los estándares deseados.
Un obstáculo importante es la falta de biomateriales normalizados adecuados para los procesos de bioimpresión. Las variaciones en las propiedades de los materiales pueden dar lugar a incoherencias en las propiedades mecánicas, los índices de degradación y la biocompatibilidad de las estructuras impresas, lo que afecta a la funcionalidad y la seguridad generales. Otro problema es la viabilidad y funcionalidad de las estructuras bioimpresas. Aunque los investigadores se esfuerzan por conseguir la viabilidad celular, se dan casos en los que el proceso de impresión compromete la supervivencia y el comportamiento de las células incrustadas, sobre todo como resultado de las fuerzas mecánicas.
Además, la falta de protocolos estandarizados para caracterizar y evaluar las estructuras bioimpresas dificulta el control de calidad. Las variaciones en los criterios de evaluación dificultan la comparación de resultados entre estudios. Otro reto importante es la integración de redes vasculares funcionales en los tejidos bioimpresos para un suministro adecuado de nutrientes. Los esfuerzos por crear vasos sanguíneos funcionales se han enfrentado a una complejidad que repercute en la vascularización de tejidos más grandes, por lo que deben mejorarse las técnicas actuales. Además, diversos escenarios, como la generación de órganos humanos, suscitan preocupaciones sobre la propiedad de los órganos, el consentimiento de los pacientes y las vías de regulación. Esto hace cada vez más necesarios unos marcos éticos y normativos exhaustivos específicos para la bioimpresión.
En resumen, aunque la bioimpresión ha avanzado, los retos que plantean los biomateriales, la viabilidad celular y la caracterización ponen de manifiesto que las prácticas actuales se quedan cortas. Estos problemas subrayan la importancia de seguir trabajando en la estandarización de directrices y protocolos para mejorar la fiabilidad y coherencia de la bioimpresión. Dichos ejemplos ponen de relieve la complejidad de la bioimpresión y la necesidad de abordar los retos técnicos, éticos y normativos para establecer normas universalmente aceptadas.
¿Qué piensas de la ética entorno al uso de la bioimpresión 3D? Deja tus comentarios en nuestras redes sociales: Facebook, Twitter y Youtube. Sigue toda la información sobre impresión 3D en nuestra Newsletter semanal.
*Créditos foto de portada: Deep-image.ai







