Triastek Inc. erhält IND-Zulassung für Medikament T21 zur Behandlung von Darmerkrankrungen

Dass die Medizin innerhalb der letzten Jahre besonders durch die additive Fertigung profitieren konnte, ist mehr als offensichtlich. Neben der Herstellung von Gesichtsmasken, Prothese, Orthesen oder auch Bildungsmaterial wurde aber auch immer stärker in den Druck von Medikamenten investiert. Eines dieser Unternehmen, die sich damit beschäftigt haben, ist der chinesische Hersteller von 3D-gedruckten Arzneimitteln Triastek Inc. Seit dessen Gründung im Jahr 2015 setzen sie sich neben dem Design von Darreichungsformen ebenfalls mit der digitalen pharmazeutischen Produktentwicklung wie auch der intelligenten Fertigung auseinander – und das zum Wohle der Menschheit. Nun erhielt Triastek von der US-amerikanischen Gesundheitsbehörde FDA (Food and Drug Administration) die Zulassung für das mittels 3D hergestellte Medikament mit dem Namen T21, welches zur Behandlung von Colitis ulcerosa eingesetzt werden soll.
Colitis ulcerosa stellt eine der häufigsten chronisch-entzündlichen Darmerkrankungen dar. Betroffene Personen leiden hierbei unter einer Entzündung des Dickdarms und es kann ebenfalls zu einer starken Belastung und Einschränkung des Lebens führen. Mit dem Medikament T21 von Triastek, welches konkret eine IND-Zulassung hat – also die Einreichung neuer Prüfpräparate – und somit den ersten Schritt zum Beginn der klinischen Studien in den Vereinigten Staaten gehen kann.
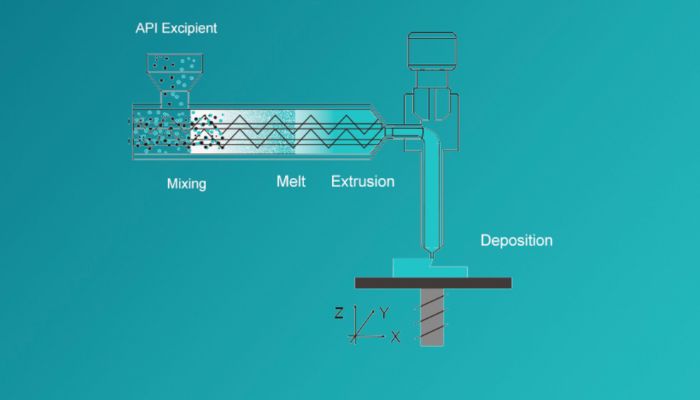
Die Abbildunng veranschaulicht das Melt-Extrusion Deposition (MED®) Verfahren (Bild: Triastek)
Wie wurde das Medikament T21 hergestellt?
Die hierbei verwendete Technologie zum 3D-Druck funktioniert mittels Schmelzextrusionsablagerung (Melt-Extrusion Deposition, MED®), bei der pulverförmige Ausgangsstoffe stets in einen weichen oder geschmolzenen Zustand geführt werden. Anschließend beginnt die Auftragung von Schicht für Schicht, bis schließlich das 3D-gedruckte Medikament T21 realisiert werden kann. Die Besonderheit, die mit der Nutzung der additiven Fertigung kommt, ist die gezielte Verabreichung des Medikaments, das für den Dickdarm gedacht ist. Hier kann das Arzneimittel das Dickdarmsegment des Magen-Darm-Trakts gezielt erreichen und ermöglicht somit auch die niedrigere Medikamentendosis bei gleichbleibender Wirkung. Außerdem war es Triastek somit möglich, radioaktive Bildgebungsmittel bereits in sehr frühen Phasen der Entwicklung des Medikaments einzusetzen. Dies bewirkt, dass der Ort der Wirkstofffreisetzung innerhalb des Magen-Darm-Trakts bewertet werden konnte. Das bedeutet schließlich für zukünftige Medikamente, dass diese bestimmte Segmente innerhalb des Magen-Darm-Trakts anvisieren können und für eine höhere Effizienz und Erfolgsquote sorgen. Schließlich gibt das Unternehmen weiters bekannt, dass diese Technologie nicht nur für Tabletten zur oralen Einnahme mit verzögerter Freisetzung genutzt werden kann, sondern auch äußerst hilfreich bei der weiteren Forschung für Peptidmedikamente sein.
„Wir freuen uns sehr, dass wir die IND-Genehmigung erhalten haben, um mit den klinischen Studien für diese potenziell transformative Behandlung für Patienten zu beginnen. Die verzögerte Freisetzung von Medikamenten und die Verabreichung von oralen Darreichungsformen an den Dickdarm ist eine Herausforderung. Daher bietet T21 eine vielversprechende neue Option für Patienten, indem es eine ortsspezifische Medikamentenverabreichung und eine lokalisierte Medikamentenwirkung ermöglicht, wodurch eventuelle Nebenwirkungen einer systemischen Exposition gemildert werden. Wir freuen uns darauf, diese Behandlung in die Kliniken zu bringen und danken der FDA für ihre Unterstützung“, gibt sich Dr. Senping Cheng, Gründer und CEO von Triastek, erfreulich.

Der Ablauf der klinischen Tests (Bild: Triastek)
Möglicherweise haben Sie bereits von vergangenen Durchbrüchen von Triastek im Bereich der additiven Medikamentenherstellung gehört, denn sie haben ebenfalls eine IND-Genehmigung für die Medikamente T19 und T20 – für die Behandlung von rheumatoider Arthritis bzw. Herz-Kreislauf- und Gerinnungsstörungen – erhalten. Wenn Sie mehr darüber erfahren möchten, dann finden Sie HIER die Pressemitteilung von Triastek.
Was halten Sie von Triastek und den 3D-gedruckten Medikament T21? Teilen Sie es uns mit und kontaktieren Sie uns. Möchten Sie eine Zusammenfassung der wichtigsten Neuigkeiten im 3D-Druck und der Additiven Fertigung direkt und bequem in Ihr Postfach? Registrieren Sie sich jetzt für unseren wöchentlichen Newsletter und folgen Sie uns auf Facebook und Twitter um stets auf dem Laufenden zu bleiben! Außerdem sind wir auch auf LinkedIN und auf Youtube zu finden.






