Behindern EU-Vorschriften den Fortschritt des medizinischen 3D-Drucks?

Der Markt für medizinischen 3D-Druck ist in den letzten Jahren stark gewachsen. Dies gilt auch für die EU, wo der gesamte AM-Markt für das Gesundheitswesen bis 2029 mit einer durchschnittlichen jährlichen Wachstumsrate von 15,4 % wachsen soll. Das ist wenig überraschend, wenn man bedenkt, dass das Europäische Patentamt im vergangenen Jahr festgestellt hat, dass die internationalen Patentfamilien im Bereich der 3D-Drucktechnologien in der Region jährlich um 26,4 % gewachsen sind, wobei fast ein Fünftel der Patente zwischen 2001 und 2020 im Gesundheitssektor angemeldet wurden. Aber gibt es Faktoren, die das Wachstum bremsen könnten?
Neue Forschungsergebnisse von Dr. Marc Mimler, Dozent in Rechtswissenschaften an der The City Law School, legen dies nahe. In dem Artikel „Core Legal Challenges for Medical 3D Printing in the EU“ (Rechtliche Herausforderungen für den medizinischen 3D-Druck in der EU) untersuchte Mimler zusammen mit anderen Mitarbeitern verschiedener Universitätskliniken und Fachbereiche des Maschinenbaus die EU-Gesetzgebung und Rechtsprechung, die unter die Medizinprodukteverordnung (Medical Device Regulation, MDR) fallen, zu Fragen der Zulassung vor dem Inverkehrbringen und der Haftung nach dem Inverkehrbringen von 3D-gedruckten Geräten. Die Ergebnisse scheinen zu zeigen, dass die Grauzonen der EU-Vorschriften das Wachstum des medizinischen 3D-Drucks tatsächlich behindern und mehr Arbeit zur Klärung der Fragen erforderlich ist.
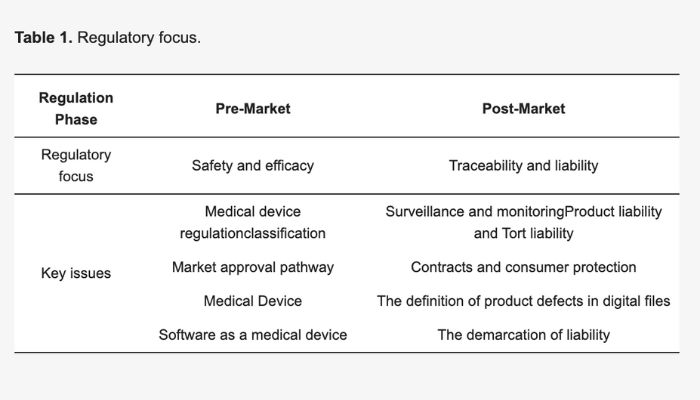
Der Schwerpunkt der Studie liegt auf den Vorschriften für 3D-gedruckte Medizinprodukte vor und nach dem Inverkehrbringen (Bild: Mimler et al.)
Studie untersucht, ob EU-Vorschriften das Wachstum des medizinischen 3D-Drucks behindern
Die Ergebnisse, die in einer Pressemitteilung der City School dargelegt werden, sind nach dem Status vor und nach dem Inverkehrbringen unterteilt. Bei der Betrachtung der Vorschriften vor dem Inverkehrbringen konzentrierten sich die Forscher auf die „Ausnahmeregelung für kundenspezifische Geräte“ der EU, die es ermöglicht, dass Geräte, die nach einer schriftlichen Beschreibung von einer autorisierten Person hergestellt werden, Anforderungen wie die CE-Kennzeichnung umgehen können. Obwohl dies für den 3D-Druck positiv zu sein scheint, schafft die Tatsache, dass „patientenangepasste“ Produkte (die für einen bestimmten Patienten hergestellt wurden) nicht unter diese Regelung fallen, eine Grauzone für 3D-gedruckte Medizinprodukte. Zumal es diese Unterscheidung für „massengefertigte“ Produkte nicht gibt.
Infolgedessen ist die Einhaltung der EU-Vorschriften für Produkte, die mithilfe der additiven Fertigung hergestellt werden, ungewiss. Diese Verwirrung wird noch dadurch verstärkt, dass die industrielle Fertigung von 3D-gedruckten Produkten in Gesundheitseinrichtungen und Krankenhäusern zwar unter die Ausnahmeregelung der MDR für Gesundheitseinrichtungen fallen kann, dies aber nicht für andere Unternehmen gilt. Das macht es für Einrichtungen und kleinere Unternehmen schwierig, sich im Vorschriften-Dschungel für maßgeschneiderte 3D-gedruckte Produkte zurechtzufinden.
Das betrifft nur die Zulassung vor dem Inverkehrbringen, aber auch die Vorschriften nach dem Inverkehrbringen scheinen für den 3D-Druck im Gesundheitswesen unklar zu sein. Aufgrund des strengeren Ansatzes der EU bei der Überwachung und Kontrolle von Medizinprodukten nach dem Inverkehrbringen ist die Produkthaftung für 3D-gedruckte Geräte nach der Medizinprodukteverordnung unklar. Dies ist darauf zurückzuführen, dass die Grenze zwischen medizinischer Fahrlässigkeit und Produkt unscharf ist.
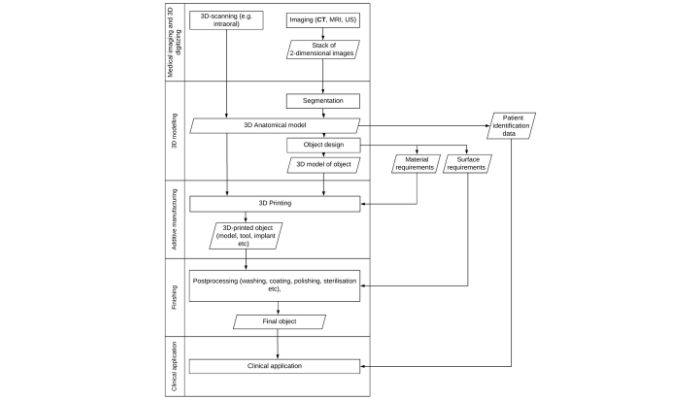
Die dezentralisierte Natur des Prozesses für 3D-gedruckte Medizinprodukte (wie oben gezeigt) kann zu Verwirrung und Problemen bei den EU-Vorschriften nach dem Inverkehrbringen führen (Bild: Mimler et al.)
Dies, so argumentieren die Autoren, hemmt die Innovation in diesem Bereich, da Parteien wie Chirurgen, Dritthersteller und interne Hersteller für etwaige Mängel nach der Implantation eines 3D-gedruckten Objekts in einen Patienten haftbar gemacht werden könnten. Und die Verwirrung ist eine direkte Folge der Tatsache, dass aufgrund der dezentralen Natur des 3D-Drucks nicht klar ist, wer genau der Hersteller ist. Die Unsicherheit in Bezug auf den Datenschutz und die Gesetze zum Schutz des geistigen Eigentums machen die Sache nur noch komplizierter.
Alles in allem stellen die Forscher fest, dass es wichtig ist, die ihrer Meinung nach konservativen und unklaren Anforderungen der Medizinprodukteverordnung in Bezug auf 3D-gedruckte Produkte zu überdenken. Sie argumentieren, dass das System und die vielen EU-Vorschriften derzeit Innovationen in diesem Bereich behindert. Dies verzögert dann die Versorgung neuer Patienten, da die Akteure möglicherweise nicht in der Lage sind, sich in der aktuellen Regulierungsszene für maßgeschneiderte Produkte zurechtzufinden. Weitere Informationen finden Sie HIER.
Was denken Sie? Können die EU-Vorschriften den Fortschritt des 3D-Drucks behindern? Lassen Sie uns dazu einen Kommentar da, oder teilen Sie es uns auf Facebook oder LinkedIN mit. Möchten Sie außerdem eine Zusammenfassung der wichtigsten Neuigkeiten im 3D-Druck und der additiven Fertigung direkt und bequem in Ihr Postfach erhalten? Dann registrieren Sie sich jetzt für unseren wöchentlichen Newsletter.






